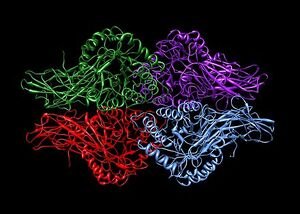
Beta-Glucuronidasa
La β-glucuronidasa es una enzima que está presente en gran cantidad de tejidos y por ser responsable de la degradación de glucosaminoglucanos.
Las beta-glucuronidasas son miembros de la familia de enzimas de las glicosidasas que catalizan la descomposición de los carbohidratos complejos . La β-glucuronidasa humana es un tipo de glucuronidasa (un miembro de la familia 2 de las glicosidasas) que cataliza la hidrólisis de los residuos de ácido β-D- glucurónico del extremo no reductor de los mucopolisacáridos (también denominados glicosaminoglicanos ) como el heparán sulfato. La β-glucuronidasa humana se encuentra en el lisosoma . En el intestino, la β-glucuronidasa del borde en cepillo convierte la bilirrubina conjugada en la forma no conjugada para su reabsorción. La β-glucuronidasa también está presente en la leche materna, lo que contribuye a la ictericia neonatal. La proteína está codificada por el gen GUSB en humanos y por el gen uidA en bacterias.
Estructura
La β-glucuronidasa humana se sintetiza como un monómero de 80 kDa (653 aminoácidos ) antes de que la proteólisis elimine 18 aminoácidos del extremo C-terminal para formar un monómero de 78 kDa. La beta-glucuronidasa existe como un homotetrámero de 332 kDa . La beta-glucuronidasa contiene varias formaciones estructurales notables, incluido un tipo de barril beta conocido como barril de rodillo de gelatina y un barril TIM.
Mecanismo de catálisis
La β-glucuronidasa humana es homóloga a la enzima β-galactosidasa de Escherichia coli. Esta relación homóloga, junto con el conocimiento de que las glicosidasas a menudo realizan hidrólisis catalizada por dos residuos ácidos, permitió el desarrollo de una hipótesis mecanicista. Esta hipótesis propone que los dos residuos de ácido glutámico Glu540 y Glu451 son los residuos nucleofílico y ácido, respectivamente, y que el residuo de tirosina Tyr504 también está implicado en la catálisis. En apoyo de esta hipótesis, las mutaciones experimentales en cualquiera de estos tres residuos dan como resultado grandes disminuciones de la actividad enzimática. El aumento de la actividad de una enzima mutante E451A (donde Glu451 se reemplaza con un residuo de alanina) después de la adición de azida es consistente con Glu451 como residuo ácido / base. Mediante el análisis de péptidos de β-glucuronidasa marcados después de la hidrólisis de un sustrato que entra en una etapa intermedia muy estable, los investigadores han determinado que Glu540 es el residuo nucleófilo.
Referencias:
Jain S, Drendel WB, Chen ZW, Mathews FS, Sly WS, Grubb JH (abril de 1996). "La estructura de la beta-glucuronidasa humana revela candidatos lisosomales dirigidos y motivos de sitio activo". Biología estructural de la naturaleza . 3 (4): 375–81. doi : 10.1038 / nsb0496-375 . PMID 8599764 . S2CID 28862883 .
440px-Beta-Glucuronidase_Homotetramer.jpg
Homotetramero de glucuronidasa (unidad biológica asumida)